
Немета́ллы — химические элементы, как правило, не обладающие свойствами металлов. Занимают правый верхний угол Периодической системы элементов Менделеева и обычно отделены линией (лесенкой). Количество неметаллов составляет 22-23 элемента, в зависимости от классификации.

Ксено́н — химический элемент 18-й группы, пятого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 54.

Триокси́д ксено́на XeO3 — белые или светло-голубые кристаллы. Получают гидролизом тетра- или гексафторида ксенона. В сухом виде чрезвычайно взрывоопасен, особенно при контакте с органикой.

Тетрафтори́д ксено́на — соединение ксенона со фтором, представляющее собой при комнатной температуре бесцветные кристаллы со слабым желтоватым оттенком и чрезвычайно высокой химической активностью и агрессивностью. Самое устойчивое соединение ксенона. Чистый тетрафторид ксенона стабилен, однако во влажном воздухе гидролизуется с образованием оксифторидов ксенона.

Гексафтори́д ксено́на — XeF6, бинарное неорганическое химическое соединение ксенона с фтором, представляющее собой при комнатной температуре бесцветные кристаллы. Формально является высшим фторидом ксенона. Обладает чрезвычайно высокой химической активностью и агрессивностью.

Тетраокси́д ксено́на XeO4 — жёлтые кристаллы при температуре ниже −36 °C. XeO4 — соединение ксенона, в котором ксенон проявляет высшую степень окисления +8 (такую степень окисления ксенон может проявить только в соединении с кислородом, максимальная степень окисления со фтором равна +6, например, в гексафториде ксенона) и соответственно валентность, равную 8. Кроме него такую же степень окисления ксенон имеет в ксеноновой кислоте и её солях.

Дифторид ксенона XeF2 — твёрдое плотное кристаллическое соединение белого цвета, образованное атомами фтора и ксенона. Одно из самых устойчивых соединений ксенона.
Фториды ксенона — бесцветные кристаллы с резким специфическим запахом. Ксенона фториды — сильные окислители. Окислительная способность уменьшается в ряду: XeF6>XeF4>XeF2. Фториды ксенона раздражают и обжигают кожу и слизистые оболочки; ПДК 0,05 мг/м³.

Окси́д-тетрафтори́д ксено́на(VI) (оксотетрафтори́д ксено́на), XeOF4 — неорганическое соединение ксенона с кислородом и фтором. Бесцветная жидкость. Растворим в безводном HF. Гидролизуется с образованием XeO2F2 и ХеО3. Проявляет амфотерные свойства, образуя, например, Cs+XeOF−5, XeOF3AsF−6, XeOF4·XeOF3+SbF−6, 2XeOF4·VF5. При контакте с кожей вызывает сильные ожоги.
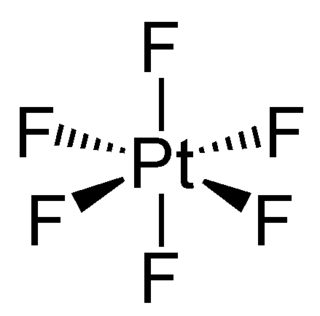
Фторид платины(VI) PtF6 (гексафторид платины) — химическое соединение платины и фтора. Платина в этом соединении находится в высшей степени окисления. Представляет собой тёмно-красные летучие кристаллы.
Нил Ба́ртлетт — химик, открывший соединения благородных газов.

Ксеноновая кислота — соединение благородного газа.

Марганца(II) фторид— неорганическая соль марганца и плавиковой кислоты, образует слабо-розовые кристаллы.
Фтори́д зо́лота(V) — красно-коричневое кристаллическое вещество, химическая формула  . Может рассматриваться как неорганическое соединение золота и фтора или как золотая соль плавиковой кислоты.
. Может рассматриваться как неорганическое соединение золота и фтора или как золотая соль плавиковой кислоты.
Изотопы ксенона — разновидности химического элемента ксенона, имеющие разное количество нейтронов в ядре. Известны изотопы ксенона с массовыми числами от 108 до 147, и более 10 ядерных изомеров.

Ксено́новая кислота́ — очень неустойчивое химическое соединение с формулой  .
.
Гептафторксенат(VI) цезия — CsXeF7, неорганическое комплексное соединение цезия, имеющее ионное строение: (Cs+)(XeF7−). Соединение благородного газа ксенона.
Бис(пентафтортеллуроксид) ксенона(IV) (тефлат ксенона(IV), пентафтортеллурат(VI) ксенона(IV)) Xe(OTeF5)4 — одно из неорганических соединений ксенона, со связью ксенон-кислород.
Перксенаты — неорганические соли четырехосновной ксеноновой кислоты MenXeO6.

Окси́д-дифтори́д ксено́на (химическая формула — XeOF2) — сложное неорганическое соединение ксенона с кислородом и фтором.














