Термодина́мика — раздел физики, изучающий наиболее общие свойства макроскопических систем и способы передачи и превращения энергии в таких системах.
Свобо́дная эне́ргия Ги́ббса — это величина, изменение которой в ходе химической реакции равно изменению внутренней энергии системы. Энергия Гиббса показывает, какая часть от полной внутренней энергии системы может быть использована для химических превращений или получена в их результате в заданных условиях и позволяет установить принципиальную возможность протекания химической реакции в заданных условиях. Математически это термодинамический потенциал следующего вида:

Гомеоста́з — саморегуляция, способность открытой системы сохранять постоянство своего внутреннего состояния посредством скоординированных реакций, направленных на поддержание динамического равновесия. Стремление системы воспроизводить себя, восстанавливать утраченное равновесие, преодолевать сопротивление внешней среды.
Хими́ческая термодина́мика — раздел физической химии, изучающий процессы взаимодействия веществ методами термодинамики. Применение термодинамического подхода к химическим реакциям основано на том, что в фундаментальном уравнении Гиббса в качестве переменных можно использовать как массы или количества независимых компонентов, — если условия задачи не требуют детального рассмотрения химического равновесия, — так и массы (количества) составляющих веществ совместно с уравнениями связи, описывающими химические реакции, — когда требуется подробное описание химического равновесия.
Термодинами́ческое равнове́сие — состояние системы, при котором остаются неизменными во времени макроскопические величины этой системы в условиях изолированности от окружающей среды.
Пра́вило фаз — соотношение, связывающее число компонентов, фаз и термодинамических степеней свободы в равновесной термодинамической системе. Роль правила фаз особенно велика при рассмотрении гетерогенных равновесий в многофазных многокомпонентных системах.
Положи́тельная обра́тная связь (ПОС) — тип обратной связи, при котором изменение выходного сигнала системы приводит к такому изменению входного сигнала, которое способствует дальнейшему отклонению выходного сигнала от первоначального значения, то есть знак изменения сигнала обратной связи совпадает со знаком изменения входного сигнала.
Внутренняя энергия термодинамической системы может изменяться двумя способами: посредством совершения работы над системой и посредством теплообмена с окружающей средой. Энергия, которую получает или теряет система (тело) в процессе теплообмена с окружающей средой, называется коли́чеством теплоты́ или просто теплотой. Теплота — это одна из основных термодинамических величин в классической феноменологической термодинамике. Количество теплоты входит в стандартные математические формулировки первого и второго начал термодинамики.

Критическая точка фазового равновесия — точка на диаграмме состояния веществ, соответствующая критическому состоянию, то есть конечная точка кривой сосуществования фаз, в котором две фазы, находящиеся в термодинамическом равновесии, становятся тождественными по своим свойствам. В частности, с приближением к критическому состоянию различия в плотности, составе и других свойствах сосуществующих фаз, а также теплота фазового перехода и межфазное поверхностное натяжение уменьшаются, а в критической точке равны нулю. В окрестности критической точки наблюдаются критические явления.
При́нцип Ле Шателье́ — Бра́уна (1884 г.) — если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий равновесия, то в системе усиливаются процессы, направленные в сторону противодействия изменениям.
Химическое равновесие — состояние химической системы, в которой протекает одна или несколько химических реакций, причём скорости в каждой паре прямой-обратной реакции равны между собой. Для системы, находящейся в химическом равновесии, концентрации реагентов, температура и другие параметры системы не изменяются со временем.
Равнове́сие Нэ́ша — концепция решения, одно из ключевых понятий теории игр. Так называется набор стратегий в игре для двух и более игроков, в котором ни один участник не может увеличить выигрыш, изменив свою стратегию, если другие участники своих стратегий не меняют. Джон Нэш доказал существование такого равновесия в смешанных стратегиях в любой конечной игре.

Эффекти́вность по Паре́то — такое состояние системы, при котором ни один показатель системы не может быть улучшен без ухудшения какого-либо другого показателя.

Калори́метр — прибор для измерения количества теплоты, выделяющейся или поглощающейся в каком-либо физическом, химическом или биологическом процессе. Термин «калориметр» был предложен А. Лавуазье и П. Лапласом (1780).
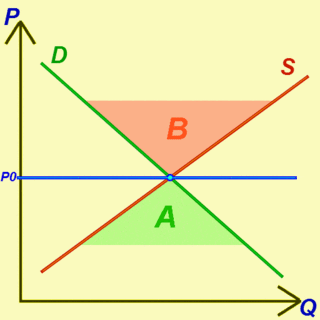
Экономи́ческое равнове́сие — состояние экономики, при котором произведенная продукция реализована, а спрос удовлетворен в условиях, когда имеющиеся трудовые ресурсы и производственные мощности используются в полном объёме, а нарушаемые пропорции быстро восстанавливаются. В экономике, экономическое равновесие характеризует состояние, в котором экономические силы сбалансированы и, в отсутствие внешних воздействий, (сбалансированные) величины экономических переменных не будут изменяться.
Тепловой эффект химической реакции — изменение внутренней энергии  или энтальпии
или энтальпии  системы вследствие протекания химической реакции и превращения исходных веществ (реактантов) в продукты реакции в количествах, соответствующих уравнению химической реакции при следующих условиях:
системы вследствие протекания химической реакции и превращения исходных веществ (реактантов) в продукты реакции в количествах, соответствующих уравнению химической реакции при следующих условиях:
- единственно возможной работой при этом является работа против внешнего давления,
- как исходные вещества, так и продукты реакции имеют одинаковую температуру.
Термодинамическое состояние — совокупность макроскопических параметров, характеризующих состояние термодинамической системы. Выбор параметров конкретной термодинамической системы зависит от целей исследования, связь между параметрами носит название уравнения состояния. Количество независимых параметров, выделяемых среди всех описывающих термодинамическое состояние, называется числом термодинамических степеней свободы. Термодинамические состояния делятся на равновесные и неравновесные, изучаемыми в рамках соответствующих теорий.
Химическая переменная — в физической химии величина, которая отражает полноту протекания реакции, то есть то, на сколько изменился состав системы в ходе реакции.
Стационарное состояние — состояние термодинамической системы, при котором значения термодинамических величин — температуры, давления, химического потенциала компонента смеси, массовой скорости — во всех частях системы остаются неизменными во времени. Зависимость от времени хотя бы одной термодинамической величины служит признаком нестационарности состояния. Стационарное состояние может быть как равновесным, так и неравновесными. Последнее реализуются лишь тогда, когда между термодинамической системой и её окружением имеют место процессы переноса, а термодинамические силы, и, как следствие, термодинамические потоки на границах системы поддерживают постоянными.











