
Синдро́м Аспе́ргера — общее нарушение психического развития, характеризующееся серьёзными трудностями в социальном взаимодействии, а также ограниченным, стереотипным, повторяющимся репертуаром интересов и занятий. От детского аутизма он отличается прежде всего тем, что речевые и когнитивные способности в целом сохраняются. Синдром часто характеризуется также выраженной неуклюжестью.

Лиссэнцефалия — аномалия развития: сглаживание извилин коры больших полушарий головного мозга, возникающее в результате недостаточной миграции нейробластов из первичной нервной трубки. При лиссенцефалии может наблюдаться агирия — отсутствие извилин мозга.
Синдро́м Мюнхга́узена — симулятивное расстройство, при котором человек преувеличенно изображает (симулирует) или искусственно вызывает у себя симптомы болезни, чтобы подвергнуться медицинскому обследованию, лечению, госпитализации, хирургическому вмешательству и т. п. Причины такого симулятивного поведения полностью не изучены. Общепринятое объяснение причин синдрома Мюнхгаузена гласит, что симуляция болезни позволяет людям с этим синдромом получить внимание, заботу, симпатию и психологическую поддержку, которых им не хватает.

Reeler — мышь-мутант, в организме которой не вырабатывается белок рилин. Наследование мутации имеет аутосомно-рецессивный характер. Отсутствие рилина приводит к нарушению миграции нейронов и дезорганизации слоев коры мозга. У мыши reeler слои коры мозга практически инвертированы, выстраиваясь «снаружи внутрь». Гипоплазия мозжечка приводит к пошатывающейся походке, благодаря которой мышь получила своё название. В субвентрикулярной и субгранулярной зонах мозга у мыши reeler нарушена миграция нейробластов. Исследование мышей reeler позволяет изучить механизмы нейрогенеза и построения мозга и нарушения этих процессов.

Рецептор липопротеинов очень низкой плотности по структуре схож с рецептором липопротеинов низкой плотности, но не способен связывать липопротеины низкой плотности. Рецептор VLDLR играет роль в метаболизме липопротеинов очень низкой плотности. Экспрессия VLDLR высока в сердце, скелетных мышцах, жировой ткани; VLDLR совместно с рецептором LDLR связывает и захватывает остаточные липопротеины: липопротеины промежуточной плотности и хиломикронные ремнанты.

Синдром мышечной скованности — крайне редкий неврологический синдром неясной этиологии, при котором у пациента нарастает общая скованность мышц.

Матриксная металлопротеиназа 2 - одна из протеиназ внеклеточного матрикса человека, кодируемая геном MMP2 на 16-й хромосоме.
Синдро́м лиссэнцефали́и Ми́ллера — Ди́кера — редкое нарушение развития по причине делеции нескольких генов в локусе 17p13. Нарушение развития мозга проявляется в лиссэнцефалии и снижении числа кортикальных слоёв с шести до четырёх. Также заметно изменение формы лица, отмечается замедленный рост, множественные патологии сердца, почек, ЖКТ.
Митохондриальная тРНК лейцина 1 — тРНК человека, кодируемая митохондриальным геном MT-TL1. Представляет собой молекулу транспортной РНК длиной в 75 нуклеотидов, основной функцией MT-TL1 является перенос остатка аминокислоты лейцина к растущей полипептидной цепочке при трансляции митохондриальных мРНК на рибосомах митохондрий.

Синдром MELAS — прогрессирующее нейродегенеративное заболевание, характеризующееся проявлениями, перечисленными в названии, и сопровождается полиморфной симптоматикой — диабетом, судорогами, снижением слуха, сердечными заболеваниями, низким ростом, эндокринопатиями, непереносимостью физических нагрузок и нейропсихиатрическими отклонениями. В каждом конкретном случае набор симптомов и их тяжесть может сильно отличаться, поскольку синдром связан с мутациями во многих генах: MTTL1, MTTQ, MTTH, MTTK, MTTS1, MTND1, MTND5, MTND6, MTTS2. Мутации могут возникать впервые у конкретного пациента, либо наследоваться по материнской линии. Всего к 2009 году было обнаружено 23 миссенсных точечных мутаций и 4 делеции мтДНК, приводящих к MELAS, однако продолжаются сообщения о новых пациентах с симптомами расстройства при отсутствии известных мутаций.

Идиопатическая кальцификация базальных ганглиев 1 характеризуется накоплением кальция в различных областях мозга, преимущественно в базальных ганглиях. Деградация функций нервной системы у пациентов с синдромом становится заметной в возрасте от 30 до 50 лет, но может появиться в детстве или в более позднем возрасте.
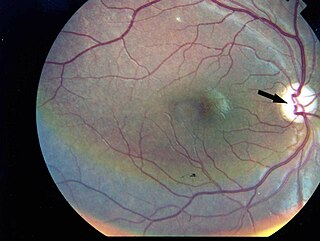
DIDMOAD-синдро́м — аутосомно-рецессивно наследуемый синдром, ассоциированный с инсулинозависимым сахарным диабетом и прогрессирующей атрофией диска зрительного нерва, которые выявляют до 16-летнего возраста. Сочетается с двусторонней прогрессирующей нейросенсорной тугоухостью, несахарным диабетом центрального генеза, дисфункцией автономной нервной системы, приводящей к развитию нейропатического мочевого пузыря и другим проявлениям нейродегенерации, включающими мозжечковую атаксию, миоклональную эпилепсию и атрофию ствола головного мозга. Развёрнутая клиническая картина (фенотипически) встречается приблизительно у 75 % пациентов. Сахарный диабет неаутоиммунного генеза, клинические проявления недостаточности инсулина проявляются приблизительно в 6-летнем возрасте. Средняя продолжительность жизни достигает 30 лет, в течение этого срока происходит развитие полного фенотипа данного синдрома.
Система антигенов Kell — группа антигенов на поверхности эритроцитов, являющихся важными детерминантами крови и служащих мишенью для многих аутоиммунных или аллоиммунных заболеваний, уничтожающих эритроциты. Показатель Kell обозначается как K, k и Kp. Антигены Kell представляют собой пептиды, обнаруженные в белке kell, 93 кДа трансмембранной цинко-зависимой эндопептидазе, которая отвечает за расщепление эндотелина-3.
Синдро́м Ке́рнса — Се́йра (англ. Kearns–Sayre syndrome, сокращённо KSS) — митохондриальная миопатия с типичным началом до 20-летнего возраста. KSS является более серьёзным синдромным вариантом хронической прогрессирующей внешней офтальмоплегии, синдром, который характеризуется изолированным поражением мышц, контролирующих движения век и контролирующих движения глаз. Это приводит к птозу и офтальмоплегии соответственно. KSS включает в себя триаду уже описанных CPEO, двустороннюю пигментную ретинопатию и блокаду сердца. Другие области участия могут включать в себя мозжечковую атаксию, проксимальную мышечную слабость, глухоту, сахарный диабет, дефицит гормона роста, гипопаратиреоз или другие эндокринные нарушения. В обоих этих заболеваниях вовлечение мышц может начаться односторонним, но всегда развивается в двусторонний дефицит, который является прогрессирующим.
Синдром Неймегена является редким аутосомно-рецессивным наследственным синдромом хромосомной нестабильности, при котором наблюдается микроцефалия, иммунодефицит и склонность к злокачественным новообразованиям. Синдром Неймегена вызван мутациями в гене NBN, который участвует в клеточном ответе на повреждения ДНК.
Трихотиодистрофия (TTD) — аутосомно-рецессивное наследственное заболевание, характеризующееся ломким волосом и интеллектуальными нарушениями. TTD связана с диапазоном симптомов, затрагивающих органы эктодермы и нейроэктодермы. TTD могут быть подразделены на четыре синдрома: Примерно половина всех пациентов с трихотиодистрофией страдают светочувствительностью, которая делит классификацию синдромов с ней или без неё; BIDS и PBIDS, IBIDS и PIBIDS. Современное использование включает TTD-P (светочувствительная) и TTD.
Синдром Коккейна , также называемый синдром Нил-Дингуолл — редкое аутосомно-рецессивное, нейродегенеративное расстройство, характеризующееся недостатком роста, нарушением развития нервной системы, аномальной чувствительностью к солнечному свету (фотосенсибилизация), заболеваниями глаз и преждевременным старением. Нездоровый вид и неврологические расстройства являются критериями для диагностики, а светочувствительность, нарушения слуха и ненормальные глаза — другие весьма общие черты. Возможны проблемы любого или всех внутренних органов. Это связано с группой расстройств, называемых лейкодистрофия. В основе расстройства лежит дефект механизма репарации ДНК. Интересно, в отличие от других дефектов репарации ДНК, пациенты с CS не предрасположены к раку или инфекции. Синдром Коккейна редок, но это разрушительная болезнь, которая, как правило, приводит к смерти в первом или втором десятилетии жизни. Мутация специфических генов в синдроме Коккейна известна, но широко распространенные эффекты и его отношения с репарацией ДНК еще не очень хорошо исследованы.

УДФ-глюкуронозилтрансфераза 1-1, также известная как UGT-1A, является ферментом, кодируемым геном UGT1A1.
Синдром задержки фазы сна — хроническое расстройство циркадного ритма, проявляющееся в виде очень позднего засыпания и позднего пробуждения с невозможностью сместить время сна на более ранние часы. Помимо времени сна, у пациентов смещены ритмы выработки гормонов и ритм температуры тела.
Синдром WAGR – это редкий наследственный аутосомно-доминантный синдром (частота 1:500000—1:1000000 человек, который клинически характеризуется сочетанием опухоли Вильмса, аниридии, урогенитальных аномалий и/или гонадобластомы и задержки психомоторного развития. Синдром встречается примерно в 8 % случаев врожденной аниридии, и в 0,75% всех случаев опухоли Вильмса.









