
Систе́ма комплеме́нта — комплекс защитных белков, постоянно присутствующих в крови. Это каскадная система протеолитических ферментов, предназначенная для гуморальной защиты организма от действия чужеродных агентов, она участвует в реализации иммунного ответа организма. Является важным компонентом как врождённого, так и приобретённого иммунитета. Выделяют три основных пути активации системы комплемента: классический, альтернативный и лектиновый. Для запуска классического пути комплемента необходима опсонизация чужеродной клетки антителами, а альтернативный и лектиновый пути могут активироваться в отсутствие антител. Поздние стадии у всех трёх путей активации системы комплемента одинаковы и включают образование мембраноатакующего комплекса, который нарушает целостность мембраны клетки-патогена и приводит к её гибели.

Кле́точное ядро́ — окружённая двумя мембранами важная структура эукариотической клетки. В клетках прокариот ядра нет. В клетках эукариот обычно одно ядро, однако некоторые типы клеток, например, эритроциты млекопитающих, не имеют ядра, а другие содержат несколько ядер.
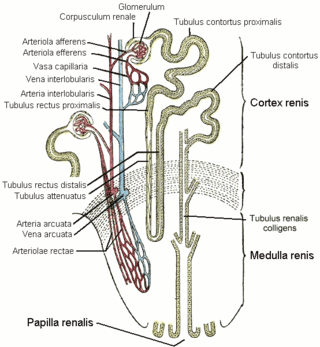
Нефрон — структурно-функциональная единица почки. Нефрон состоит из почечного тельца, где происходит фильтрация, и системы канальцев, в которых осуществляются реабсорбция и секреция веществ.

Надпо́чечники — парные эндокринные железы, расположенные над верхней частью почек позвоночных животных и человека.

По́чка — парный фасолевидный орган, очищающий кровь, выполняющий посредством функции мочеобразования регуляцию химического гомеостаза организма. Входит в систему органов мочевыделения
Тельца Вайбеля — Паладе — особые везикулы в клетках сосудистого эндотелия, которые содержат фактор фон Виллебранда и P-селектин и секретируют их в случае активации эндотелия при повреждении ткани. Могут быть сферической, овальной или продолговатой формы.
Синуклеины — семейство белков, обнаруживаемых в нервной ткани и в некоторых видах опухолей. У человека известно три белка: альфа-синуклеин, бета-синуклеин, гамма-синуклеин. В последнее время к семейству относят белок синоретин. Интерес к данным белкам пробудился после обнаружения мутации гена альфа-синуклеина в нескольких семьях с аутосомо-доминантной формой болезни Паркинсона. Пока что синуклеины обнаружены только у позвоночных, однако по структуре они схожи с LEA-белками растений . Таким образом, семейство синуклеинов насчитывает 4 изоформы.
Паренхимато́зные диспротеино́зы — дисметаболические процессы с преимущественным нарушением обмена белков, развивающиеся первично в паренхиматозных клетках органов.

Протеинопла́сты — тип пластид — лейкопластов, запасающие белки. Белки запасаются в них в виде кристаллов, кроме того, протеинопласты могут быть точками ферментативной активности, в которую вовлечены содержащиеся в них белки. Хотя все пластиды содержат белки в высоких концентрациях, только в протеинопластах, как было выяснено в 1960-х и 1970-х годах, содержатся крупные белковые включения, видимые как в световой, так и в электронный микроскоп. До сих пор неизвестно, специализируются ли они исключительно на запасании белков, подобно тому как амилопласты запасают крахмал и элайопласты — жиры.

Те́льце Каха́ля (ТК) — образование в ядре клетки, присутствующее у некоторых ядерных организмов. Типичный размер телец Кахаля составляет 1—2 мкм, и в одной клетке может содержаться от 0 до 10 ТК. Клетки многих типов не имеют ТК, но ТК имеются в ядрах нейронов и раковых клеток. Основная функция телец Кахаля заключается в процессинге малых ядерных и малых ядрышковых РНК, а также сборке рибонуклеопротеиновых комплексов.

Деменция с тельцами Леви : предположительно является второй после болезни Альцгеймера по частоте среди нейродегенеративных деменций. Согласно нейропатологическим исследованиям, деменция с тельцами Леви (ДТЛ) определялась в приблизительно 30 % случаев всех деменций.
Нейродегенеративные заболевания — группа в основном медленно прогрессирующих, наследственных или приобретённых заболеваний нервной системы. Общим для этих заболеваний является прогрессирующая гибель нервных клеток (нейродегенерация), ведущая к различным неврологическим симптомам — прежде всего, к деменции и нарушению движений. Заболевания могут наступить в различном возрасте, протекают диффузно или генерализированно, гистологически определяется специфический тип изменений.

UniProt — открытая база данных последовательностей белков. Консорциум UniProt действует с 2003 года. Единая база данных UniProt была создана путём объединения нескольких баз. UniProt состоит из четырёх крупных баз данных и охватывает различные аспекты анализа белковых последовательностей. Многие из последовательностей стали известны в результате реализации проектов секвенирования геномов последних лет. Кроме того, база данных UniProt содержит большое количество информации о биологических функциях белков, полученной из научной литературы.
Тельца включения — это нерастворимые белковые агрегаты, образующиеся при суперэкспрессии рекомбинантных белков у бактерий.

PML-тельца́ — сферические тельца диаметром 0,1—1,0 мкм, имеющиеся в ядрах клеток многих тканей и большинства линий и входящие в состав ядерного матрикса. Ключевой организующий компонент PML-телец — белок PML, который привлекает в PML-тельца множество разнообразных белков, которые объединяет только способность подвергаться сумоилированию. В тельцах PML белки подвергаются посттрансляционным модификациям, которые приводят к изоляции белков в PML-тельцах, активации или деградации. По морфологическим признакам выделяют несколько подтипов PML-телец, причём все они характеризуются наличием электроноплотной оболочки и внутренней коровой части.

Апика́льное те́льце — особое мультивезикулярное образование на растущем кончике гифы высших грибов (Dikarya), центр её роста и морфогенеза. Это сложное, состоящее из многих белковых комплексов и везикул образование можно обнаружить на кончике растущей гифы, в местах ветвления мицелия или в прорастающей споре. В зарубежой научной литературе для обозначения этой структуры используется немецкий термин Spitzenkörper. Апикальное тельце — часть эндомембраной системы, характерная только для грибов. Основная её функция — обеспечивать поляризованный рост септированного мицелия.
Я́дерные тельца́ — субкомпартменты внутри ядра, не окружённые мембранами, но представляющие собой отдельные, морфологически различимые комплексы белков и РНК. К числу ядерных телец относят ядрышко, тельце Кахаля и другие немембранные структуры. В основе биогенеза ядерных телец лежат одни и те же общие принципы, такие как способность к формированию de novo, самоорганизация, а также роль РНК как структурного элемента. Контроль биогенеза ядерных телец необходим для правильного изменения архитектуры ядра в ходе клеточного цикла и лежит в основе ответа клетки на внутри- и внеклеточные стимулы. Многие ядерные тельца осуществляют специфические функции — например, синтез и процессинг пре-рибосомных РНК в ядрышке, накопление и сборку компонентов сплайсосом в ядерных спеклах или накопление молекул РНК в параспеклах. Механизмы, которые обеспечивают выполнение ядерными тельцами этих функций, очень разнообразны. В некоторых случаях ядерное тельце может служить местом протекания определённых процессов, например, транскрипции. В других случаях ядерные тельца, по-видимому, опосредованно регулируют локальные концентрации своих компонентов в нуклеоплазме. Хотя большинство ядерных телец имеет сферическую форму, большинство из них можно идентифицировать по уникальной морфологии, которая выявляется при помощи электронной микроскопии, и по расположению в ядре. Подобно цитоплазматическим органеллам, ядерные тельца содержат специфический набор белков, которые определяют их структуру на молекулярном уровне.

Я́дерные спе́клы, или спе́клы, или B-снурпосо́мы, или компа́ртменты фа́кторов спла́йсинга, или доме́ны SC-35, или кла́стеры интерхромати́новых гра́нул — ядерные тельца, регулирующие сплайсинг. В ядерных спеклах находятся факторы сплайсинга и малые ядерные рибонуклеопротеины. Изменения в белковом составе и функционировании ядерных спекл приводят к изменениям в альтернативном сплайсинге пре-мРНК, поэтому считается, что ключевой функцией ядерных спекл является регуляция доступности факторов сплайсинга в сайтах транскрипции. Недавние исследования показали, что в ядерных спеклах также находятся белки, задействованные в регуляции локализации хромосом, модификации хроматина, транскрипции, процессинге 3'-концов транскриптов, модификации мРНК, белки, полностью покрывающие мРНК, и мРНК-рибонуклеопротеины, поэтому ядерные спеклы рассматриваются как крупнейшие центры регуляции всех этапов экспрессии ядерных генов.
Те́льце гисто́новых ло́кусов — ядерное тельце, представляющее собой скопление факторов транскрипции генов, кодирующих гистоны, и созревания гистоновых пре-мРНК. К числу таких факторов относят белок NPAT, необходимый для транскрипции генов гистонов, а белок FLASH и малый ядерный рибонуклеопротеин U7 необходим для процессинга гистоновых пре-мРНК. Тельца гистоновых локусов обнаружены в клетках млекопитающих и дрозофилы. В клетках амфибий аналогичные ядерные тельца носят название C-снурпосома.

Класси́ческий пу́ть актива́ции систе́мы комплеме́нта — один из трёх путей активации системы комплемента, наряду с альтернативным путём и лектиновым путём. Классический путь запускают комплексы антиген-антитело, причём антитела должны принадлежать к классу IgG или IgM. После активации происходит сборка белкового комплекса C3-конвертазы (C4b2b), который разрезает белок комплемента C3. Один из фрагментов C3, C3b, связывается с C3-конвертазой, в результате чего образуется C5-конвертаза (C4b2b3b). C5-конвертаза разрезает компонент комплемента 5, после чего образовавшиеся белковые фрагменты привлекают фагоциты в очаг инфекции и способствуют поглощению клеток патогенов. C5-конвертаза также запускает финальные стадии каскада комплемента, которые завершаются формированием мембраноатакующего комплекса. Он формирует поры в мембране клетки микроорганизма, вызывая её лизис и гибель. Помимо микробных клеток, классический путь комплемента могут запускать апоптотические тельца и некротизированные клетки.













