
Ци́кл трикарбо́новых кисло́т (сокр. ЦТК, цикл Кре́бса, цитра́тный цикл, цикл лимо́нной кислоты́) — центральная часть общего пути катаболизма, циклический биохимический процесс, в ходе которого ацетильные остатки (СН3СО-) окисляются до диоксида углерода (CO2). При этом за один цикл образуется 2 молекулы CO2, 3 НАДН, 1 ФАДH2 и 1 ГТФ (или АТФ). Электроны, находящиеся на НАДН и ФАДH2, в дальнейшем переносятся на дыхательную цепь, где в ходе реакций окислительного фосфорилирования образуется АТФ.
Дыхательная цепь переноса электронов, также электрон-транспортная цепь (сокр. ЭТЦ, англ. ETC, Electron transport chain) — система трансмембранных белков и переносчиков электронов, необходимых для поддержания энергетического баланса. ЭТЦ поддерживает баланс за счёт переноса электронов и протонов из НАД∙Н и ФАДН2 в акцептор электронов. В случае аэробного дыхания акцептором может быть молекулярный кислород (О2). В случае анаэробного дыхания акцептором могут быть NO3−, NO2−, Fe3+, фумарат, диметилсульфоксид, сера, SO42−, CO2 и т. д. ЭТЦ у прокариот локализована в ЦПМ, у эукариот — на внутренней мембране митохондрий. Переносчики электронов расположены в порядке уменьшения сродства к электрону, то есть по своему окислительно-восстановительному потенциалу, где у акцептора самое сильное сродство к электрону. Поэтому транспорт электрона на всём протяжении цепи протекает самопроизвольно с выделением энергии. Выделение энергии в межмембранное пространство при переносе электронов происходит ступенчато, в виде протона (H+). Протоны из межмембранного пространства попадают в протонную помпу, где наводят протонный потенциал. Протонный потенциал преобразуется АТФ-синтазой в энергию химических связей АТФ. Сопряжённая работа ЭТЦ и АТФ-синтазы носит название окислительного фосфорилирования.
Анаэробное дыхание — это биохимический процесс окисления органических субстратов или молекулярного водорода с использованием в дыхательной ЭТЦ в качестве конечного акцептора электронов вместо O2 других окислителей неорганической или органической природы. Как и в случае аэробного дыхания, выделяющаяся в ходе реакции свободная энергия запасается в виде трансмембранного протонного потенциала, использующегося АТФ-синтазой для синтеза АТФ.

Окисли́тельное фосфорили́рование — метаболический путь, при котором энергия, образовавшаяся при окислении питательных веществ, запасается в митохондриях клеток в виде АТФ. Хотя различные формы жизни на Земле используют разные питательные вещества, АТФ является универсальным соединением, в котором запасается энергия, необходимая для других метаболических процессов. Почти все аэробные организмы осуществляют окислительное фосфорилирование. Вероятно, широкому распространению этого метаболического пути способствовала его высокая энергетическая эффективность по сравнению с анаэробным брожением.

Цитохром-c-оксида́за (цитохромоксидаза) или цитохром-c-кислород:оксидоредуктаза, также известная как цитохром aa3 и комплекс IV — терминальная оксидаза аэробной дыхательной цепи переноса электронов, которая катализирует перенос электронов с цитохрома с на кислород с образованием воды. Цитохромоксидаза присутствует во внутренней мембране митохондрий всех эукариот, где её принято называть комплекс IV, а также в клеточной мембране многих аэробных бактерий.
Кофермент В, Coenzyme B — это кофермент, принимающий участие в окислительно-восстановительных реакциях у метаногенов. Молекула кофермента В содержит тиол, который принимает участие в механизме реакции.

Кише́чная па́лочка — вид грамотрицательных палочковидных бактерий, широко распространённых в нижней части кишечника теплокровных животных. Большинство штаммов E. coli являются безвредными, однако серотип O157:H7 может вызывать тяжёлые пищевые отравления у людей и животных. Безвредные штаммы являются частью нормальной флоры кишечника человека и животных. Кишечная палочка приносит пользу организму хозяина, например, синтезируя витамин K, а также предотвращая развитие патогенных микроорганизмов в кишечнике.
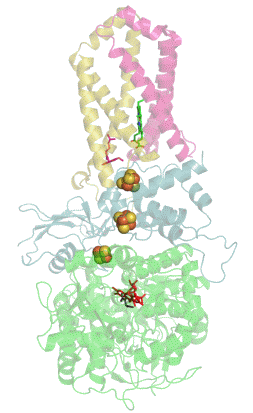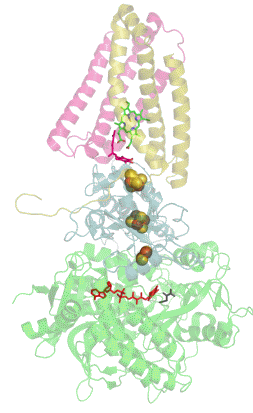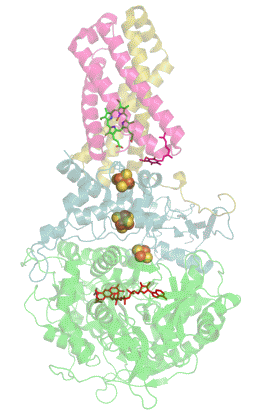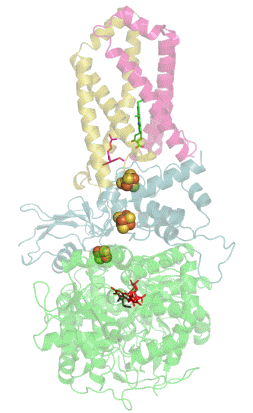
Сукцинатдегидрогеназа или сукцинат-убихинон-оксидорекдуктаза, также известная как комплекс II — белковый комплекс, расположенный во внутренней мембране митохондрий и мембранах многих прокариотических организмов. Одновременно участвует в цикле трикарбоновых кислот и дыхательной цепи переноса электронов.
Холофермент ДНК-полимеразы III — главный ферментативный комплекс, задействованный в репликации ДНК у прокариот. Он был открыт Томасом Корнбергом и Малькольмом Гефтером в 1970 году. Комплекс обладает высокой процессивностью. У кишечной палочки E. coli он функционирует вместе с четырьмя другими ДНК-полимеразами, IV, V). Кроме полимеразной, холофермент может также корректировать возникающие при репликации ДНК ошибки за счёт 3'→5'-экзонуклеазной активности. Он входит в состав крупного ферментативного комплекса, осуществляющего репликацию ДНК — реплисомы.

Глиоксила́тный цикл, или глиоксила́тный шунт — анаболический путь, имеющийся у растений, бактерий, протистов и грибов, представляет собой видоизменённый цикл трикарбоновых кислот. Глиоксилатный цикл служит для превращения ацетил-СоА в сукцинат, который далее используется для синтеза углеводов. У микроорганизмов он обеспечивает утилизацию простых углеродных соединений в качестве источника углерода, когда более сложные источники, например, глюкоза, недоступны, а также может считаться одной из анаплеротических реакций цикла трикарбоновых кислот, восполняющей количества сукцината и малата. Считается, что у животных глиоксилатный цикл отсутствует, однако в последние годы в некоторых тканях животных были обнаружены ключевые ферменты цикла — малатсинтаза и изоцитратлиаза.

Фотосисте́ма I, или пластоциани́н-ферредокси́н-оксидоредукта́за — второй функциональный комплекс электрон-транспортной цепи (ЭТЦ) хлоропластов. Он принимает электрон от пластоцианина и, поглощая световую энергию, формирует сильный восстановитель П700, способный через цепь переносчиков электронов осуществить восстановление НАДФ+. Таким образом, при участии ФСI синтезируется источник электронов (НАДФН) для последующих реакций восстановления углерода в хлоропластах в цикле Кальвина. Кроме того, ФСI может осуществлять циклический транспорт электронов, сопряжённый с синтезом АТФ, обеспечивая дополнительный синтез АТФ в хлоропластах.

Сульфитредуктаза (шифр КФ 1.8.99.1) — важный фермент, участвующий в метаболизме серы. Он катализирует восстановление сульфита до сероводорода и воды. Электроны для реакции поставляются от таких восстановительных эквивалентов как НАДФН, связанных флавиновых групп, или ферредоксина (у растений). По свойствам и строению фермент похож на нитритредуктазу.
- SO32− (сульфит) + донор электронов
 H2S (сероводород) + окисленный донор + 3 H2O
H2S (сероводород) + окисленный донор + 3 H2O

ГАМК-оперон несет ответственность за превращение γ-аминобутирата (ГАМК) в сукцинат. ГАМК -оперон включает три структурных гена - gabD , gabT и gabP , которые кодируют сукцинат полуальдегида дегидрогеназы, ГАМК-трансаминазы и ГАМК-пермеазы соответственно. Существует регулирующий ген csiR, ниже оперона, который кодирует предполагаемый репрессор транскрипции и активируется при ограничении азота.
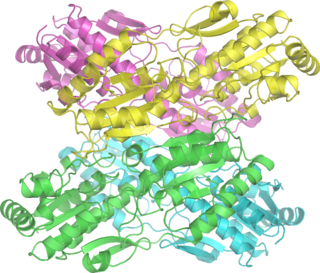
Фосфофруктокиназа-1 — фермент-фосфофруктокиназа, один из наиболее важных регуляторных ферментов. Отвечает за важный этап гликолиза, катализируя перенос фосфатной группы от молекулы АТФ к фруктозо-6-фосфату, в результате чего образуется фруктозо-1,6-бисфосфат и АДФ.

НАДН-дегидрогена́зный ко́мплекс, также называемый ко́мплекс I или НАДН-убихино́н-оксидоредукта́за — первый мультибелковый комплекс дыхательной цепи переноса электронов. Множество копий комплекса расположены в мембранах прокариотических организмов, способных к кислородному дыханию и внутренних мембранах митохондрий эукариотических клеток. По отношению к белкам человека комплекс I часто называют НАДН-дегидрогеназой.
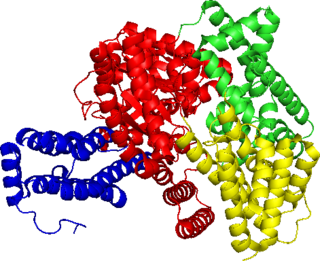
Фосфоенолпируваткарбоксилаза представляет собой фермент из семейства карбоксилаз, который встречается у растений и некоторых бактерий. Он катализирует присоединение бикарбоната (НСО3−) к фосфоенолпирувату (ФЕП) с образованием четырёх углеродного соединения оксалоацетата и неорганического фосфата:
- ФЕП + НСО3− → оксалоацетат + Фн

RecBCD — фермент бактерии Escherichia coli, инициирующий процесс гомологичной рекомбинации при репарации двух- и одноцепочечных повреждений молекулы ДНК, возникающих в результате ионизирующего излучения, ошибок в процессе репликации, ошибок в работе эндонуклеаз или в результате окислительного стресса. RecBCD — это одновременно и хеликаза, раскручивающая двойную спираль ДНК, и нуклеаза, которая её разрезает.
Ферредоксин-НАДФ+-редуктаза, сокращенно ФНР, фермент из класса оксидоредуктаз, катализирующий реакцию восстановления НАДФ+, используя в качестве донора электронов ферредоксин.
Сукцинат-полуальдегид-дегидрогеназа (НАДФ+) (Шифр КФ 1.2.1.79, Дегидрогеназа янтарного полуальдегида (НАДФ+), сукцинат-полуальдегид-дегидрогеназа (НАДФ+), сукцинат полуальдегид:НАДФ+ оксидоредуктаза, НАДФ-зависимая сукцинат-полуальдегид-дегидрогеназа, GabD) — фермент, систематическое название которого сукцинат-полуальдегид:НАДФ+ оксидоредуктаза. Фермент катализирует следующую химическую реакцию:
- сукциниловый полуальдегид + НАДФ+ + Н2О
 сукцинат + НАДФН + 2 H+
сукцинат + НАДФН + 2 H+

Вне́шняя бактериа́льная мембра́на, или нару́жная бактериа́льная мембра́на — биологическая мембрана, располагающаяся поверх слоя пептидогликана у грамотрицательных бактерий. По составу она отличается от внутренней, клеточной мембраны. На её поверхности находятся липополисахариды, являющиеся антигенами грамотрицательных патогенных бактерий.
![Структура димера хинол-фумаратредуктазы[1]](https://upload.wikimedia.org/wikipedia/commons/thumb/8/8b/PDB_2bs3_EBI.jpg/274px-PDB_2bs3_EBI.jpg)














