Термодина́мика — раздел физики, изучающий наиболее общие свойства макроскопических систем и способы передачи и превращения энергии в таких системах.
Свобо́дная эне́ргия Ги́ббса — это величина, изменение которой в ходе химической реакции равно изменению внутренней энергии системы. Энергия Гиббса показывает, какая часть от полной внутренней энергии системы может быть использована для химических превращений или получена в их результате в заданных условиях и позволяет установить принципиальную возможность протекания химической реакции в заданных условиях. Математически это термодинамический потенциал следующего вида:

Термодинамическая энтропия  , часто именуемая просто энтропией, — физическая величина, используемая для описания термодинамической системы, одна из основных термодинамических величин; энтропия и температура — сопряжённые термодинамические величины, необходимые для описания термических свойств системы и тепловых процессов в ней. Энтропия является функцией состояния и широко используется в термодинамике, в том числе технической и химической.
, часто именуемая просто энтропией, — физическая величина, используемая для описания термодинамической системы, одна из основных термодинамических величин; энтропия и температура — сопряжённые термодинамические величины, необходимые для описания термических свойств системы и тепловых процессов в ней. Энтропия является функцией состояния и широко используется в термодинамике, в том числе технической и химической.
Уравне́ние Арре́ниуса устанавливает зависимость константы скорости  химической реакции от температуры
химической реакции от температуры  .
.
Хими́ческая реа́кция — превращение одного или нескольких исходных веществ (реагентов) в другие вещества (продукты), при котором ядра атомов не меняются, при этом происходит перераспределение электронов и ядер, и образуются новые химические вещества. В отличие от ядерных реакций, при химических реакциях не изменяется общее число ядер атомов и изотопный состав химических элементов.
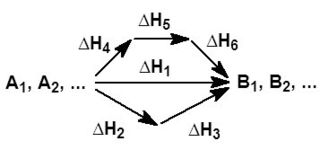
Закон Гесса — основной закон термохимии, который формулируется следующим образом:
- Тепловой эффект химической реакции, проводимой в изобарно-изотермических или изохорно-изотермических условиях, зависит только от вида и состояния исходных веществ и продуктов реакции и не зависит от пути её протекания.
Уравне́ние состоя́ния — соотношение, отражающее для конкретного класса термодинамических систем связь между характеризующими её макроскопическими физическими величинами, такими как температура, давление, объём, химический потенциал, энтропия, внутренняя энергия, энтальпия и др. Уравнения состояния необходимы для получения с помощью математического аппарата термодинамики конкретных результатов, касающихся рассматриваемой системы. Эти уравнения не содержатся в постулатах термодинамики, так что для каждого выбранного для изучения макроскопического объекта их либо определяют эмпирически, либо для модели изучаемой системы находят методами статистической физики. В рамках термодинамики уравнения состояния считают заданными при определении системы. Если изучаемый объект допускает термодинамическое описание, то это описание выполняют посредством уравнений состояния, которые для реальных веществ могут иметь весьма сложный вид.
Термодинами́ческое равнове́сие — состояние системы, при котором остаются неизменными во времени макроскопические величины этой системы в условиях изолированности от окружающей среды.
Термохи́мия — раздел химической термодинамики, в задачу которой входит определение и изучение тепловых эффектов реакций, а также установление их взаимосвязей с различными физико-химическими параметрами. Ещё одной из задач термохимии является измерение теплоёмкостей веществ и установление их теплот фазовых переходов.

Экзотерми́ческая реа́кция — химическая реакция или ядерная реакция, сопровождающаяся выделением теплоты. По знаку тепловыделения противоположна эндотермической реакции — реакции с поглощением теплоты.
Парадо́кс Ги́ббса — отсутствие непрерывности для энтропии при переходе от смешения различных газов к смешению тождественных газов, когда, например, при переходе от бесконечно мало отличающихся идеальных газов к тождественным расчётное значение энтропии смешения падает скачком до нуля, что представляется неожиданным и нелогичным.
Тепловой эффект химической реакции — изменение внутренней энергии  или энтальпии
или энтальпии  системы вследствие протекания химической реакции и превращения исходных веществ (реактантов) в продукты реакции в количествах, соответствующих уравнению химической реакции при следующих условиях:
системы вследствие протекания химической реакции и превращения исходных веществ (реактантов) в продукты реакции в количествах, соответствующих уравнению химической реакции при следующих условиях:
- единственно возможной работой при этом является работа против внешнего давления,
- как исходные вещества, так и продукты реакции имеют одинаковую температуру.
Гибридизация ДНК, гибридизация нуклеиновых кислот — соединение in vitro комплементарных одноцепочечных нуклеиновых кислот в одну молекулу. При полной комплементарности объединение происходит легко и быстро, а в случае частичной некомплементарности слияние цепочек замедляется, что позволяет оценить степень комплементарности. Возможна гибридизация ДНК-ДНК и ДНК-РНК.
Уравнение Брёнстеда — уравнение, количественно описывающее зависимость скорости катализируемых кислотами или основаниями реакций от природы катализатора. Впервые установлено в 1924 году Брёнстедом и Педерсеном.
Конста́нта равнове́сия — величина, определяющая для данной химической реакции соотношение между термодинамическими активностями исходных веществ и продуктов в состоянии химического равновесия. Зная константу равновесия реакции, можно рассчитать равновесный состав реагирующей смеси, предельный выход продуктов, определить направление протекания реакции.

Реальный раствор — гомогенная смесь двух или более компонентов, образование которой сопровождается тепловым эффектом и изменением объема. Это объясняется различной Ван-дер-Ваальсовой энергией межмолекулярного взаимодействия между однородными и разнородными молекулами.
В химии, молекула испытывает напряжение, когда её химическая структура подвергается некоторой деформации, вызванной действием внутренних сил, которая ведёт к увеличению внутренней энергии по сравнению с эталонным соединением без деформаций. Внутренняя энергия молекулы состоит из суммы всех энергий, «запасенных» внутри неё. Отдельно взятая форма напряженной молекулы, отличающаяся от всех других называется конформером. Напряженная молекула имеет дополнительную энергию, которую не имеет ненапряженное соединение. Эту дополнительную энергию, или энергию напряжения, можно сравнить со сжатой пружиной. Точно также, как сжатая пружина должна удерживаться на месте, чтобы не дать высвободиться своей потенциальной энергии, молекула может удерживаться в энергетически невыгодной конформации за счет химических связей внутри нее. Без этих химических связей, удерживающих конформер на месте, энергия напряжения сразу бы высвободилась.
В термодинамике спонтанный (самопроизвольный) процесс — это процесс, который происходит без какого-либо внешнего воздействия на систему. Более техническое определение: спонтанный процесс — это эволюция системы во времени, при которой она высвобождает свободную энергию и переходит в более низкое, более термодинамически стабильное энергетическое состояние. Соглашение о знаках для изменения свободной энергии следует общему соглашению для термодинамических измерений, в котором высвобождение свободной энергии из системы соответствует отрицательному изменению свободной энергии системы и положительному изменению свободной энергии среды.


























